【中国上海、苏州、成都,近日】易慕峰生物,一家致力于突破实体瘤治疗的免疫细胞治疗产品开发企业,在第 28 届美国基因与细胞治疗学会(ASGCT)年会上,凭借其自主研发的基于慢病毒载体的 In Vivo CAR-T创新性技术平台精彩亮相,该平台通过全新的设计,打破了该领域的专利壁垒,取得了具有明显优势的体内外特异性和有效性,为肿瘤免疫治疗提供了全新策略。
ASGCT现场壁报展示
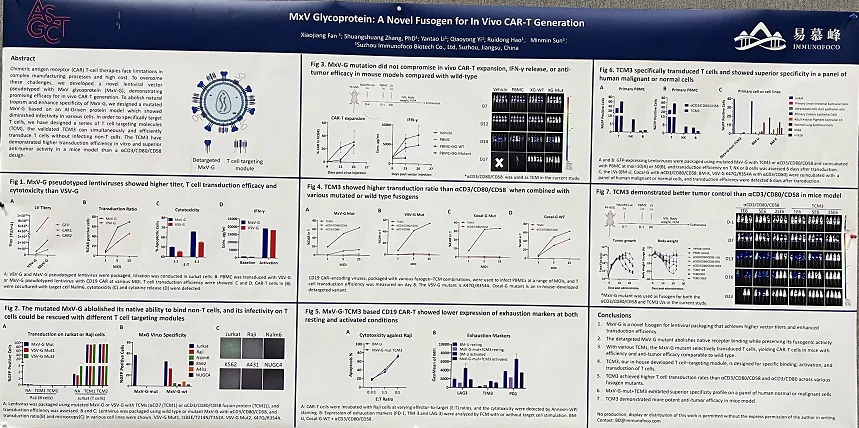
新型慢病毒载体:打破专利壁垒,实现多维度优势
易慕峰团队开发的以 MxV 糖蛋白(MxV-G)为假型的新型慢病毒载体,在体内 CAR-T 细胞生成方面表现出色。相较于传统VSV-G假型慢病毒载体,MxV-G 在病毒滴度、T 细胞转导效能和杀伤活性等关键性能指标上均展现出明显优势,不仅提高了病毒载体的产量和感染效率,还能更有效地识别并杀死肿瘤细胞。这一新型包膜在传统ex vivo CAR-T以及in vivo CAR-T均有良好的临床应用潜力。
AI 驱动优化:成功构建精准靶向突变体
为消除 MxV-G 的自然嗜性并增强特异性,团队利用人工智能驱动的蛋白质模型,成功设计并构建了突变型 MxV-G 。突变后的MxV-G消除了对非T细胞的感染性,同时保留了其介导膜融合的活性。通过引入不同的 T 细胞靶向模块,恢复了其对 T 细胞的感染能力,实现了精准靶向,提高了治疗的安全性和有效性。
新一代T细胞靶向分子:特异性与抗肿瘤活性双升级
为精准靶向 T 细胞,团队设计了多种T细胞靶向分子(TCM),其中,经过验证的 TCM3 能够高效地转导T细胞,同时不感染非T细胞。进一步的,TCM3 与各种突变型或野生型的膜融合蛋白联合使用时,展现出比αCD3/CD80/CD58 (MDF)以及αCD3/CD80更高的转导效率。基于MxV-G-TCM3 的 CAR-T 细胞在多种细胞系中展现出高特异性。此外,实验证明其耗竭标志物表达更低,有助于维持 T 细胞活性,增强长期抗肿瘤效果;进一步小鼠模型实验也证明了其体内抗肿瘤活性显著优于 αCD3/CD80/CD58。
易慕峰生物合伙人、研发中心负责人郝瑞栋博士表示:"CAR-T细胞疗法虽为癌症治疗带来革命性突破,但复杂的个体化生产工艺与高昂成本制约其广泛应用。基于慢病毒的in vivo CAR-T平台由于其良好的临床前数据,近两年成为行业发展的新趋势。我们开发的全新In Vivo技术平台,一方面打破了国外企业在膜融合蛋白(Fusogens)和T细胞靶向分子部分的专利壁垒,另一方面展示出了具有明显优势的体内外特异性和有效性。我们希望通过这些成果,降低治疗成本,简化制造过程,让更多肿瘤患者能从中受益。未来,我们的研发团队会继续深入探索这项技术的应用潜力,推动其临床应用。"
易慕峰是一家致力于突破实体瘤治疗,给全球患者带来长期生存获益的免疫细胞治疗药物开发企业。公司由科学家和产业精英合作组建,于2020年9月启动运营,核心成员成功推动了中国首个CAR-T药物的上市申请,具有丰富的细胞药物开发和产业化经验。
易慕峰从实体瘤治疗痛点和临床获益出发,在全球范围内首次提出“化实体瘤为血液瘤”的临床策略,并在此基础上开发了Peri Cruiser®技术平台,同时还开发了SNR、T-Booster等技术平台,旨在提高CAR-T产品的安全性、对抗肿瘤异质性以及提高其扩增和浸润肿瘤的能力。
公司始终以临床价值为导向,拥有丰富的产品管线,其中IMC002(CLDN18.2 CAR-T)获得了美国FDA授予的快速通道资格,以及胃癌和胰腺癌两项孤儿药资格认定(ODD),其IND申请已于2023年4月获得中美双报批准;IMC001(EpCAM CAR-T)已进行了两项IIT临床研究,并展示出良好可耐受的安全性和初步有效性,于2023年8月获得美国FDA ODD认定,其IND申请于2024年2月获得中美双报批准,其新增适应症IND申请于2025年3月获得中国CDE批准;IMC008(SNR CAR-T)已快速推进到IIT临床研究阶段,于2023年8月获得两项美国FDA ODD认定,分别用于治疗胃癌和胰腺癌。
公司秉承“众擎举易,同心执慕,勇攀高峰”的发展理念,集聚行业英才,携手开发能够给实体瘤患者带来长期生存获益的创新药物。更多信息,请访问公司网站www.immunofoco.com。