JSI-1187的I期临床试验是一项开放标签、多中心剂量递增和扩展临床研究,在携带MAPK突变的复发、难治性实体肿瘤患者中评估JSI-1187的安全性、耐受性、药代动力学、药理动力学和临床药效。该临床研究包括3个阶段:1)JSI-1187单药剂量爬坡阶段,用于实体肿瘤患者;2)JSI-1187与BRAF抑制剂达拉非尼联用的剂量爬坡;3)对携带特定基因突变肿瘤患者的扩展研究。
负责JSI-1187项目开发的首席开发官Linda Paradiso博士表示:“JSI-1187是选择性ERK1/2激酶抑制剂,我们希望通过ERK抑制剂来对抗携带MAPK通路突变的肿瘤,能够开发更有效的单药和联合疗法,在耐药产生早期阶段防止和解决目前已有的MAPK通路靶向药常见的耐药问题'。
捷思英达首席执行官张劲涛博士表示:“JSI-1187临床试验的启动对捷思英达是一个非常重要的里程碑。JSI-1187是捷思英达首个自主创新研发并进入临床研究的抗癌新药,从项目立项到进入临床试验,总共耗费约三年时间。在抗击新冠疫情,确保安全的前提下,捷思英达和合作单位共同努力,先后在美国国家癌症研究院(NCI)指定的四家综合性癌症中心启动了临床试验。我们期待JSI-1187能为肿瘤患者带来福音。”
JSI-1187是由捷思英达自主开发的口服高选择性ERK1/2小分子激酶抑制剂,在临床前模型中对MAPK 通路突变的肿瘤显示出高度抑制性。通过 RAS-RAF-MEK-ERK 级联的 MAPK 信号在癌症生长和增殖中起着至关重要的作用。MAPK/ERK 通路的突变存在于多种癌症类型中,包括胰腺癌(+90%)、胆道癌(3-50%)、结直肠癌(30-50%)、肺癌(25-30%)、卵巢癌(15-39%)和子宫内膜 (18%)中的KRAS突变,以及黑色素瘤 的NRAS突变 (20%)和BRAF V600突变(50%)等。虽然BRAF/MEK抑制剂靶向联合疗法在黑色素瘤和其他癌症中比单药具有更显著的药效,但大多数患者最终都会产生耐药性和疾病进展。在已发现的耐药机制中,关键是ERK激酶的重新激活。因此,ERK 抑制具有避免或克服耐药的潜力。
目前全球尚无ERK激酶抑制剂获批上市,进展最快的项目也仅处于II期阶段,包括优立替尼(BioMed Valley Discoveries/Vertex)、LY3214996(礼来)、LTT462(诺华)。JSI-1187于2020年1月获得美国FDA临床申请许可,2020年6月在美国启动临床I期试验(临床试验登记号为:NCT04418167)。
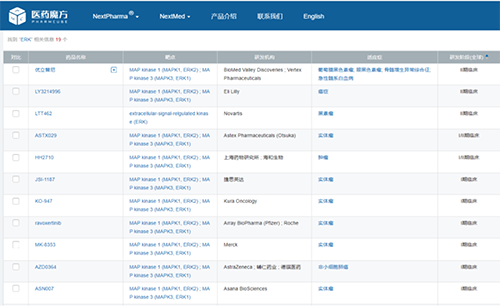
来源:NextPharma
关于捷思英达
捷思英达位于上海张江科学城国际医学园区,专注于小分子原创抗癌新药的研发。捷思英达在上海张江国际医学园区拥有包括动物房在内的新药探新研究技术平台,在美国波士顿设有负责项目引进和临床开发的子公司。捷思英达采用自主研发和项目引进齐头并进的“双轮驱动”商业模式,加快研发管线的建立。公司研发团队及时应用国际知名临床专家最新发现的药物作用机制,开展国际首创的抗癌新药研发,努力解决国内外肿瘤患者高度未满足的临床需求。