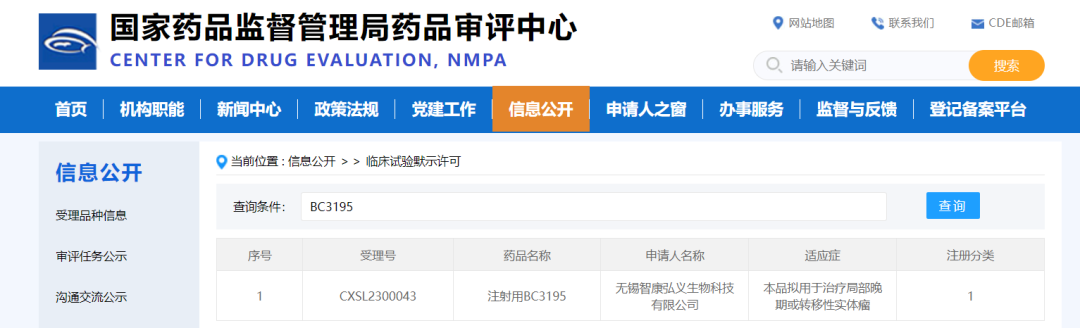
近日,智康弘义发布新闻稿称,其全球独家开发的新一代靶向CDH3的抗体偶联药物(ADC)BC3195通过国家药品监管管理局(NMPA)临床默示许可,拟用于治疗局部晚期或转移性实体瘤。
根据智康弘义新闻稿介绍,BC3195全新靶向的CDH3蛋白在多种恶性实体肿瘤(如肺癌和乳腺癌等)中特异性高表达,是理想的、具有高度潜力的可针对多种恶性实体肿瘤的ADC靶点。
作为一款最新一代全球独家靶向CDH3靶点的ADC产品,BC3195的优势之一在于采用高度差异化的抗体设计,抗体与CDH3蛋白具有较高的亲和力,同时展现出非常出色的内吞活性;BC3195的另一优势在于策略性的采用经临床验证的连接子和具有“旁观者效应”的有效载荷vcMMAE,极大的提高了临床开发的可靠性。BC3195在临床前研究中表现出优异的肿瘤抑制活性,在多个肿瘤模型中的肿瘤生长抑制率大于100%。
BC3195已于今年2月获批美国临床,智康弘义计划在中美同步开展BC3195的 I 期临床研究,广东省人民医院的吴一龙教授将担任本临床试验的主要研究者,来自美国纪念斯隆-凯特琳癌症中心(MSKCC)的肿瘤内科专家Bob Li教授将负责在美开展的临床试验。
联系方式:ir@biocitypharma.com
往期推荐:
智康弘义——WEE1激酶小分子抑制剂SC0191获批美国 I/II 临床,拟单药和联合化疗用于治疗晚期实体瘤 | 项目进展
智康弘义——全球首创新一代靶向CDH3的抗体偶联药物(ADC)获批美国临床 | 项目进展
智康弘义——TIM-3单抗BC3402注射液在中美分别获l期、Ib/II期临床试验批准,拟用于治疗恶性血液疾病 | 项目进展