CGC729(Auto):该产品是针对CD70靶点开发的AIMS CAR-NKT自体产品。目前,CGC729临床试验(IIT)在复旦大学附属肿瘤医院开展,采用单臂、剂量递增,3+3设计,评估CGC729的低、中、高剂量(DL1: 5 x106/m2; DL2: 1.5x107/m2; DL3: 4.5 x107/m2)对于肾透明细胞癌晚期复发转移患者的安全性及初步疗效。
安全性评估:截止目前已经完成了DL1和DL2组所有受试者的给药,6名受试者均未出现剂量限制性毒性(DLT),未出现大于2级的CRS和ICANS,安全性良好。
疗效评估:在可评估的5名受试者中(DL1=2,DL2=3),总体客观缓解率(ORR)达到了40%(2/5),疾病控制率(DCR)达到了100%(5/5);在CD70阳性的4名受试者中(DL1=2,DL2=2),ORR为50%(2/4),DCR为100%(4/4),且其中一名受试者PR持续响应时间截止目前长达12个月。
此外,药代动力学研究结果显示,所有受试者无论肿瘤中CD70的表达水平如何,都可以观察到CGC729在体内的强大扩增和存续,最长存续时间在血液中可长达5个月。
综上所述,这是首次CAR-NKT产品针对晚期复发转移透明细胞肾癌(R/R mRCC)患者的临床试验初步安全性和有效性数据,也是首次针对RCC采用该种疗法进行的临床试验,该结果显示了CGC729产品良好的安全性和令人鼓舞的初步抗肿瘤活性。
CGC738(Auto):该产品是针对CD70靶点开发的下一代AIMS CAR-NKT自体产品,其临床前数据显示出比CGC729更强的抗肿瘤活性和体内增殖等特点,接下来该产品临床试验的研究也会首次在肾细胞癌患者中进行。
CGC766(Auto):该产品是基于AIMS CAR-NKT平台开发的新一代双靶点CAR-NKT自体产品,是为了进一步解决实体肿瘤抗原的异质性、肿瘤抑制的免疫微环境以及体内存续较差等问题。目前正在进行临床前的研究(肾细胞癌、卵巢癌和胃癌等模型),初步数据显示双靶点CAR-NKT细胞在增殖和抗肿瘤活性等方面都具有一定的优势。
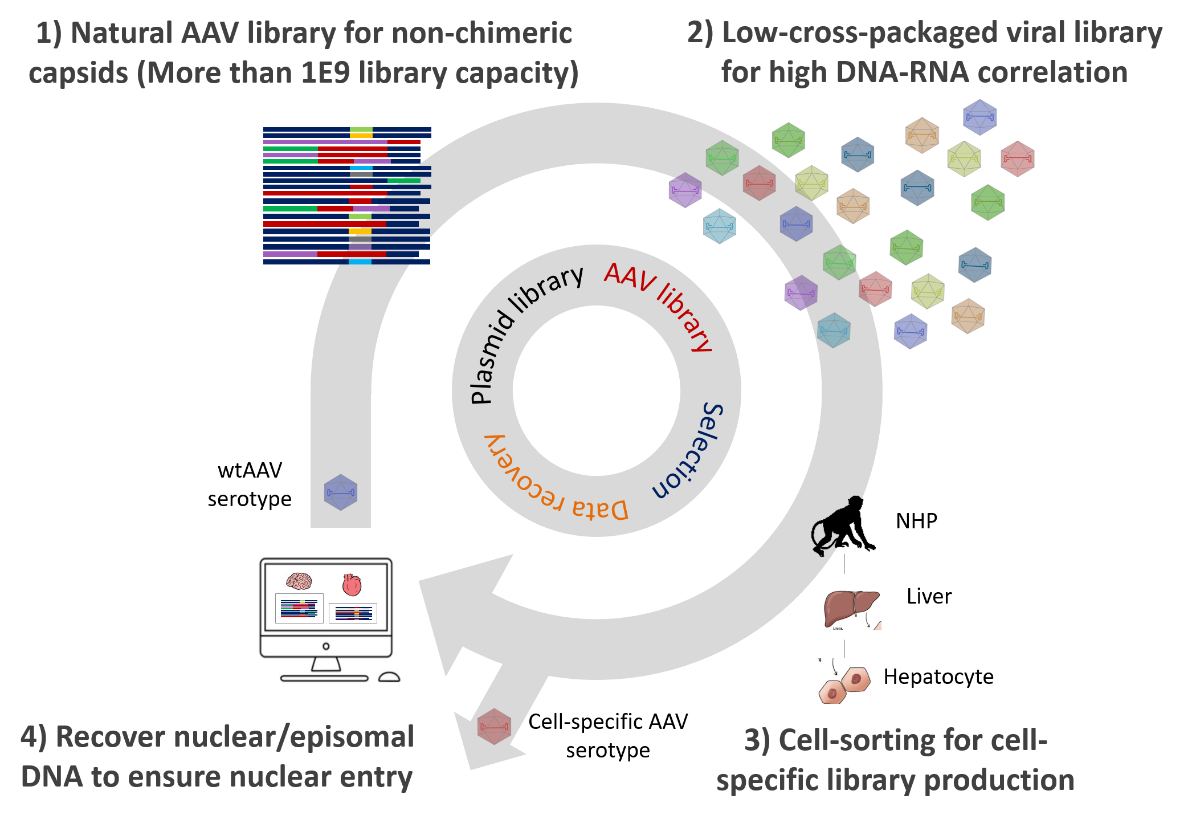
基于VELPTM平台,公司已开发多种组织/细胞靶向的AAV创新血清型。
靶向脑/神经细胞:为了更好的穿过血脑屏障(BBB)并实现神经细胞特异性的高表达,公司构建了多种类型的AAV衣壳文库,如基于不同血清型的多肽插入库、DNA shuffling文库等,并在筛选中回收并分选神经细胞核以实现细胞特异性文库。目前基于AAV9的多肽插入文库中,已获得的高感染血清型在脑部的mRNA转录水平高出AAV9约1000倍(NGS数据)。此外,DNA shuffling文库在筛选中体现了普遍更高的脑部嗜性,有望进一步提升多肽插入文库的感染活性。
靶向肝/肝实质细胞:通过2轮食蟹猴的筛选,目前已获得的肝脏高感染活性的AAV血清型数个,在与野生型AAV头对头单独包装验证实验中,其感染活性的mRNA水平高出野生型7-30倍(NGS数据)。令人惊喜的是,一些血清型在保证高感染活性的同时,体现了非常高的靶向肝的专一性,如开发的血清型肝脏靶向占96%,野生型AAV5肝脏靶向占54%(测试组织包括肝、脑、肺、心、肾、DRG、肌等)。
靶向心/心肌细胞:为了更好的筛选心脏靶向的AAV衣壳,公司构建了半理性设计的多肽插入文库,引入刚性氨基酸/环状拓扑结构等,增加心脏微环境高剪切力条件下的相互作用。在2轮食蟹猴的筛选后,目前获得心脏高感染活性的AAV血清型数十个,最优血清型高出AAV9的mRNA转导活性近40倍。
靶向肾/足细胞:肾脏的微环境复杂,细胞种类多样,其中肾足细胞与组织恢复及疾病关系密切。为了获得特异性靶向足细胞的AAV衣壳,公司优化了肾足细胞的分选方法,优化后可以在每一轮筛选中回收足细胞约60%(优化前约回收0.04%)。经过2轮食蟹猴筛选,目前以获得靶向肾脏的AAV血清型,其靶向能力超过野生血清型约300倍。
在组织/细胞精准靶向的AAV加持下,公司同时开发了组织特异性的长效治疗基因表达盒,开发能够有效并特异递送至靶细胞的新型长效精准基因治疗产品,并扩展开发针对以前AAV未能有效靶向的适应症,以满足具有巨大临床需求的罕见和普遍遗传型疾病。为此,公司已经建立了差异化基因治疗产品管线。目前公司主要聚焦于开发针对中枢神经系统疾病(如老年痴呆及遗传发育型癫痫);针对心血管疾病(如遗传性心肌病);针对肾脏疾病(如遗传性肾病综合症)等的新型一流AAV基因治疗产品,这些管线目前正在快速临床前验证以及临床转化中。

基因治疗 | 公司技术平台及研发管线
关键技术平台
细胞治疗平台AIMS CAR-NKT 基于不变的天然杀伤性T细胞(NKT),NKT细胞是一群细胞表面既有T细胞受体TCR,又有NK细胞受体的特殊T细胞亚群,它同时具有T细胞和NK细胞的抗肿瘤特征,在新一代细胞治疗的研发中越来越受到青睐。与T细胞上TCR不同的是,NKT细胞表面的TCR是一种表达不变的Vα24-Jα18 TCR α链的先天T细胞群体,它不是识别由传统MHC分子呈递的肽抗原,而是识别由非多态性的MHC-I样分子CD1d呈递的糖脂抗原。因此,基于该技术平台开发的产品也同时具有异体使用的潜质和良好的安全性等特点。
AIMS CAR-NKT拥有多种攻击肿瘤细胞的机制:
1)CAR针对肿瘤抗原;
2)不变的TCR针对表达CD1d的肿瘤细胞和与肿瘤相关的巨噬细胞(TAM);
3)NK受体(例如,NKG2D)可结合肿瘤上的NK配体;
4)CD16用于结合抗体疗法的潜在的抗体依赖性细胞毒性反应(ADCC)。AIMS CAR-NKT还具有很强的实体肿瘤浸润能力、并且通过调控肿瘤微环境从而延长CAR-NKT持续扩增的能力等。
首个以AIMS CAR-NKT平台为基础的管线产品(CGC729)已在靶向肾透明细胞癌的临床研究中展现出良好的安全性和令人鼓舞的疗效。
技术优势:拥有适应性与先天性免疫能力,肿瘤杀伤机制的多样性,调节抑制性肿瘤微环境的能力。

AAV载体进化平台VELPTM,通过构建高质量文库(低错配率、高平衡性),以组织/细胞/核的特异分选为筛选压力,并进行逐级大数据回收(组织DNA、核DNA、环状DNA、RNA),以此提高AAV进化效率并实现细胞特异性AAV的筛选。目前基于此平台, 已完成多家授权合作(如德国Boehringer Ingelheim公司、香港Frametact公司等),并积极推进靶向心、脑、肾的基因治疗产品转化。
技术优势:低错配的高质量病毒文库,全新的筛选压力,精准的细胞特异性AAV筛选。