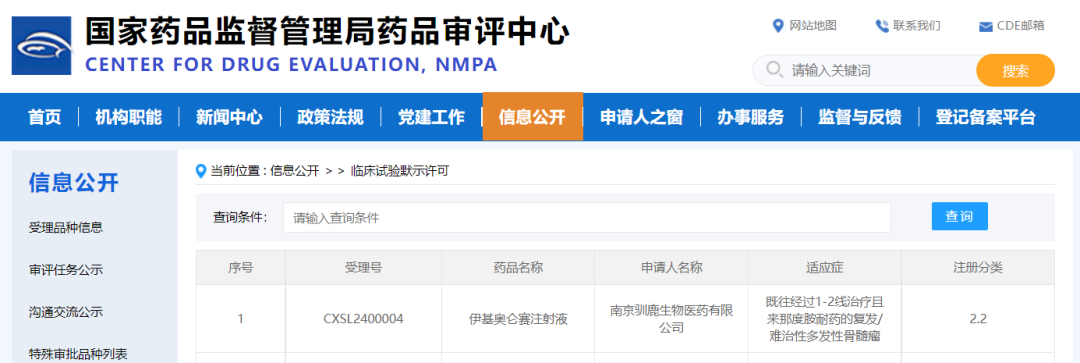
近日,中国南京、上海、美国加州圣荷西——驯鹿生物,一家致力于细胞创新药物研发、生产和销售的生物制药公司,宣布公司自主研发的全人源靶向BCMA嵌合抗原受体自体T细胞注射液(伊基奥仑赛注射液,研发代号CT103A)新药临床试验申请(IND)获中国食品药品监督管理局(NMPA)批准,拟扩大适应症用于治疗既往经过1-2线治疗且来那度胺耐药的复发/难治性多发性骨髓瘤患者。
伊基奥仑赛注射液(商品名:福可苏®)于2023年6月30日在中国上市,获批适应症为既往经过至少3线治疗后进展(至少使用过一种蛋白酶体抑制剂及免疫调节剂)的复发或难治性多发性骨髓瘤成人患者。末线治疗适应症的批准是基于一项评估伊基奥仑赛注射液治疗复发/难治性多发性骨髓瘤患者的中国多中心I/II期注册临床试验(CTR20192510, NCT05066646),FUMANBA-1的临床研究数据。
根据在2023年国际骨髓瘤学会(IMS)年会上公布的本研究最新长期随访数据,截至2022年12月31日,103例疗效可评估受试者中,总体缓解率(ORR)为96.1%,严格意义的完全缓解/完全缓解(sCR/CR)率为77.7%;91例既往无CAR-T治疗史的受试者中,ORR达98.9%,sCR/CR率达到 82.4%,12个月无进展生存(PFS)率为85.5%;94.2% (97/103) 受试者达到MRD阴性,所有CR/sCR受试者均达到MRD阴性。接受治疗的105例受试者中,仅一例受试者发生≥3级CRS,无≥3级ICANS。药代动力学数据显示,伊基奥仑赛注射液回输后能在体内长期存续,24个月时仍有40%的受试者能检测到基因拷贝数。
驯鹿生物创始人、董事长兼首席执行官张金华女士表示,“此次复发/难治性多发性骨髓瘤2-3线适应症的IND获批,是伊基奥仑赛注射液在临床开发进程中又一重大里程碑。从相关研究可以看出,RRMM患者更早线使用CAR-T治疗,生存获益更好。基于在既往临床研究中展现出的优异的有效性和安全性,相信伊基奥仑赛注射液有望填补多发性骨髓瘤早期治疗阶段巨大的临床未尽之需。我们将尽快启动临床入组工作,让更多的早期复发的患者能从该疗法中获益。”
多发性骨髓瘤(MM)是最常见的血液系统肿瘤之一,是一种克隆性浆细胞异常增殖的恶性疾病。对于初治的多发性骨髓瘤患者,常用的一线治疗包括多种药物组合的诱导治疗、巩固治疗和维持治疗,以及自体造血干细胞移植(ASCT)等。对于大多数的患者,疾病缓解后也会不可避免地进入复发、难治的治疗困局。
根据《新英格兰医学杂志》刊登的相关研究结果显示:与标准治疗方案相比,在既往接受过2-4线治疗的复发/难治性多发性骨髓瘤患者中,接受CAR-T治疗的患者无进展生存期显著延长,临床应答率明显提高[1]。在既往接受过1- 3线治疗且来那度胺耐药的复发和难治性多发性骨髓瘤患者中,接受CAR-T治疗的患者疾病进展或死亡风险低于接受标准治疗的患者[2]。
根据Globocan预测数据:中国MM的年新发病人数由2018年20,066人增至 2022年30,300人,预计2030年将增长至37,082人。美国MM的年新发病人数由2018年25,962增至2022年32,258人,预计2030年将增长至38,000人。全球MM的年新发病人数由2018年159,985增至2022年187,952人,预计2030年将增长至231,284人。
驯鹿生物是一家致力于细胞创新药物研发、生产和销售的生物制药公司。公司以开发血液肿瘤细胞类药物和抗体药物为创新基石,向自身免疫疾病拓展,拥有完整的从早期发现、临床开发、注册申报到商业化生产的全流程能力。
公司现有10余个处于不同研发阶段的创新药物品种,其中伊基奥仑赛注射液(全人源BCMA CAR-T产品)已获国家药监局(NMPA)批准上市,并已获得美国FDA批准注册临床,用于治疗复发/难治多发性骨髓瘤。
驯鹿生物凭借其强大的管理团队、创新的产品线、自有的GMP生产和超强的临床开发能力,旨在提供变革性、可治愈的创新型疗法,为中国乃至全球患者带来治愈的希望。
了解更多信息,请访问公司官网:www.iasobio.com或领英账号:www.linkedin.com/company/iasobiotherapeutics
参考文献
[1].N Engl J Med.2023 Mar 16;388(11):1002-1014
[2].N Engl J Med.2023 Jul 27;389(4):335-347