6月12日至6月15日,2024欧洲风湿病学大会(EULAR年会)在奥地利维也纳隆重召开。作为风湿病领域最具影响力的国际会议之一,全球顶尖专家紧扣临床热点和疑难问题进行探讨和分享。大会期间,一品红合作在研的全球1类新药AR882临床试验成果重磅亮相。
AR882是一种高效选择性尿酸转运蛋白(URAT1)抑制剂,旨在通过抑制URAT1使尿液尿酸盐排泄正常化,从而降低血清尿酸(sUA)水平,从而达到治疗高尿酸血症和治疗痛风的目的。目前,AR882已提前完成国内II/III期临床研究II期阶段受试者入组工作,标志着产品研发取得重大阶段性进展。
“AR882,一种可在慢性痛风关节炎患者中显著溶解痛风石的新型选择性 URAT1 抑制剂:使用游标卡尺及双能量CT(DECT)测量的全球试验12个月结果”入选本次EULAR大会报告。6月14日, Arthrosi首席医学官Robert Keenan博士在大会上报告了该研究的最新数据(摘要编号:POS0268)。研究表明:AR882在痛风石患者中进行的第6至12个月扩展研究中,患者的安全性和耐受性良好,sUA显著降低,表现出持续的痛风石和晶体体积溶解。AR882治疗痛风患者(包括临床可见及亚临床晶体沉积的患者)疗效更显著、安全性更好。
在一项随机开放的全球Ⅱ期研究中(美国,新西兰及中国台湾),试验招募了42名至少有1个皮下痛风石的患者。在实验中,患者被随机分为三组,以1:1:1的比例分别接受每日一次AR882(75mg)、AR882(50mg)+别嘌醇、别嘌醇(至多300mg)的治疗。
6个月后,别嘌醇组患者在当前治疗方案的基础上增加75mg AR882,而其他组患者则继续采用相同的方案。试验研究中,在基线、第6个月及第12个月时进行DECT成像检查。在整个研究过程中收集安全性数据,包括生命体征和心电图数据。
各组平均基线sUA水平在9.1-9.6 mg/dL之间。
第3个月,AR882 75mg组、AR882 50mg+别嘌醇组和别嘌醇组中位sUA水平分别降至4.5mg/dL、4.7mg/dL和6.1 mg/dL。第12个月,AR882 75mg、AR882 50mg+别嘌醇和AR882 75mg+别嘌醇组的sUA水平分别为4.3 mg/dL、3.7 mg/dL和2.9 mg/dL。
第6个月,在AR882 75mg组中,有4例患者(29%)测量到了痛风石的完全溶解,别嘌醇组1例(8%),AR882 50mg+别嘌醇组1例(8%)。在第6-12个月的延长期试验中,AR882 75mg组和AR882 75mg+别嘌醇组分别有4例(40.0%)和4例(36.4%)患者的痛风结石完全溶解。
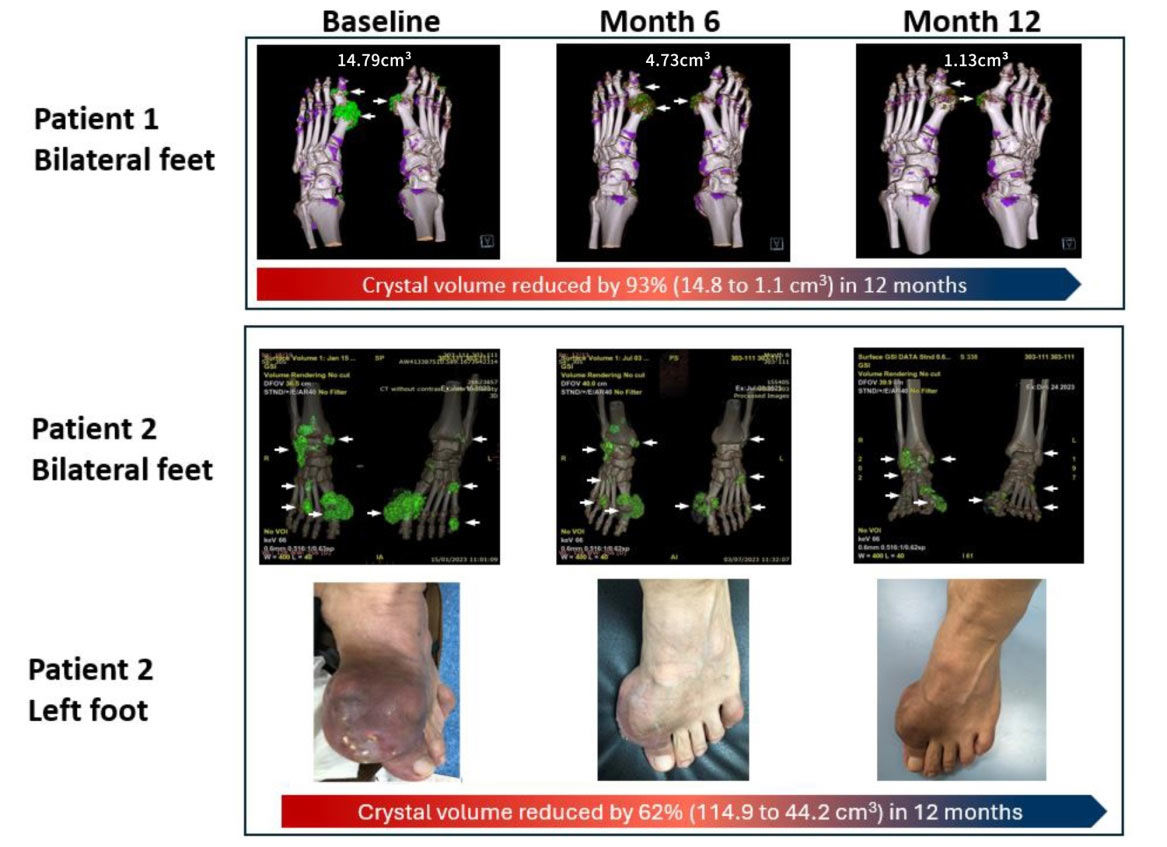
AR882 75mg单独使用或与别嘌醇联合使用显示,从基线到第6个月,总尿酸晶体体积减少;第6至12个月的拓展研究中,痛风晶体体积持续减少。
表.患者治疗后目标痛风石(≥1个)完全溶解的反应率
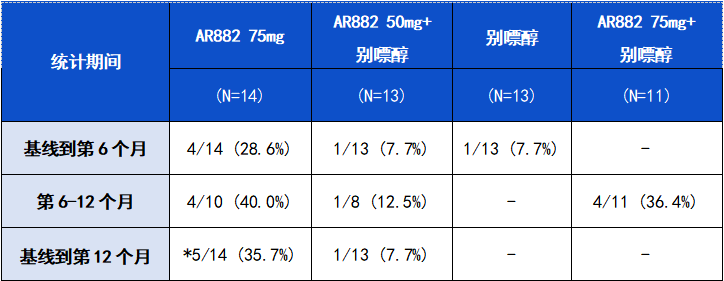
备注:*共有5名受试者在12个月内痛风石完全溶解
在整个12个月的慢性治疗中,AR882作为单一疗法或与别嘌呤醇联合治疗耐受性良好。最常见的不良事件是痛风发作,轻度或中度不良事件包括腹泻、头痛和上呼吸道感染。AR882治疗后,痛风结石率持续下降。
除上述研究外,“选择性URAT1抑制剂 AR882与肝脏、肾脏及胃肠道的关键转运蛋白均无药物相互作用”做了相应的成果展示。该研究对AR882在体外及临床研究中对转运蛋白(包括HEK293细胞表达的MATE1、MATE2-K、OATP1B1、OATP1B3、OAT1、OAT3、OCT1 和 OCT2转运蛋白,以及Caco-2细胞/膜囊中的P-gp 和 BCRP、BSEP转运蛋白)介导的药物相互作用(DDIs)潜力进行了全面评估。试验显示AR882没有表现出DDIs风险,表明AR882可以与各种主要通过转运蛋白清除的伴随药物一起在痛风患者中给药。
AR882在痛风石患者中进行的第6至12个月扩展研究中,痛风患者的安全性和耐受性良好,sUA显著降低,患者表现出持续的痛风石和晶体体积溶解。AR882有望为痛风患者(包括临床可见及亚临床晶体沉积的患者)提供更优的治疗选择。
高尿酸血症是由于血液中尿酸水平过高而引起的一种代谢性疾病,通常会导致痛风、尿酸肾病等疾病,且极易引起包括高血压、脂肪肝、慢性肾病和心脑血管等并发症。痛风与嘌呤代谢紊乱及高尿酸血症直接相关,其会在关节腔等处形成尿酸盐沉积,进而引发急性关节疼痛。痛风是由单钠尿酸盐沉积所致的晶体相关性关节病,属代谢性风湿病范畴。
高尿酸血症和痛风是一个连续、慢性的病理过程,需要长期、甚至是终生的病情监测与管理。高尿酸血症已成为继糖尿病、高血压、高血脂症后的“第四高”,痛风已成为仅次于糖尿病的第二大代谢类疾病。