近日,中国疫苗行业协会和中国标准化协会联合发布了《细胞治疗产品追溯管理信息系统基本功能规范》团体标准。《细胞治疗产品追溯管理信息系统基本功能规范》标准第一起草单位为北京百奥利盟软件技术有限公司,第一起草人为倪毅。第一起草单位和起草人组织、联合多位权威专家共同编制《细胞治疗产品追溯管理信息系统基本功能规范》,第一起草单位和起草人邀请多位业内权威专家对《细胞治疗产品追溯管理信息系统基本功能规范》进行意见征集和预审,最终形成了标准报批稿。
北京百奥利盟软件技术有限公司创始人兼总经理倪毅介绍道:”多年来,我们始终专注于生命科学数字化领域,脚踏实地,步步前行。从服务客户起步,到自主研发产品,再到编制行业标准,我们的成长与行业发展紧密相连。我们坚信,通过不断完善数字化工具,我们不仅能为客户创造价值、提供优质服务,更能推动整个行业的进步,从而实现对国家生命科学领域的数字化转型贡献力量。这是我们的使命,也是激励我们不断前进的动力。”


这一标准的制定是对国家药品监督管理局食品药品审核查验中心《细胞治疗产品生产质量管理指南(试行)》的积极响应。它为细胞治疗产品的追溯系统提供了具体的技术参考,有助于实现产品全生命周期的数字化追溯管理。这不仅有利于落实相关法规要求,也为行业的规范化发展提供了支持。
《细胞治疗产品追溯管理信息系统基本功能规范》标准编制团队和预审团队涵盖细胞治疗领域和地域广泛,包括细胞与基因数字化专家,大型生物药企的运营负责人和信息部门负责人、大型研究型医院业务负责人和信息部门负责人、细胞治疗企业负责人。
起草人和单位
倪毅(北京百奥利盟软件技术有限公司创始人/总经理)
华坚(上海医药集团生物治疗技术有限公司总经理)
邵扬(上海医药集团信息中心主任)
衡反修(北京大学肿瘤医院信息部主任)
沈东炎(厦门大学附属第一医院精准医疗中心主任)
胡欣(复旦大学附属肿瘤医院精准医疗中心主任)
罗敏(广州百暨基因科技有限公司总经理)
王婷婷(广州来恩生物医药有限公司首席运营官)
预审专家(按姓氏拼音排序)
李秀玲 (上海生物制品研究所有限责任公司总经理)
刘雅容 (沙砾生物联合创始人/CEO)
罗林云 (中国生物技术股份有限公司营销中心副总经理)
陆家海 (国家药品监督管理局疫苗及生物制品质量监测与评价重点实验室主任)
钱其军 (上海细胞治疗集团董事长兼CEO)
齐菲菲 (北京艺妙神州医药科技有限公司联合创始人/CTO)
田正隆 (高博临床研究中心首席战略官兼首席数据官)
王立群(星奕昂(上海)生物科技有限公司创始人/董事长兼CEO,副总裁袁歆代)
徐静 (中国生物研究院副院长)
张丹 (江苏谱新生物医药有限公司联合创始人)
2023年7月 标准申报-工作组讨论稿
2023年9月 合规性审查-工作组讨论稿
2024年3月 正式立项-征求意见稿
2024年3-4月 征求意见-征求意见稿
2024年4月 预审-送审讨论稿
2024年5月 会审-报批稿
2024年5月 中国生物制品大会公示-报批稿
2024年6月 结束公示
2024年7月12日 中国疫苗行业协会、中国标准化协会联合发布-正式文件


《细胞治疗产品追溯管理信息系统基本功能规范》依据《细胞治疗产品生产质量管理指南(试行)》第十一章产品追溯系统,细胞治疗产品范围包括按药品批准上市的经过适当的体外操作(如分离、培养、扩增、基因修饰等)而制备的人源活细胞产品,包括经过或未经过基因修饰的细胞,如自体或异体的免疫细胞、干细胞、组织细胞或细胞系等产品。标准适用于细胞产品从供者材料的采集、运输、接收、产品生产和检验到成品放行、储存、运输和使用的全过程。
《细胞治疗产品追溯管理信息系统基本功能规范》标准规定了细胞治疗产品追溯管理信息系统的定义、适用范围以及功能要求。标准适用于细胞治疗产品追溯管理信息系统的规划、设计、开发、应用和评价。
《细胞治疗产品追溯管理信息系统基本功能规范》标准主要内容包括:
1. 系统管理:规定了用户管理、角色权限、产品类型、审计追踪等基础功能,为系统的安全性和可追溯性奠定基础。
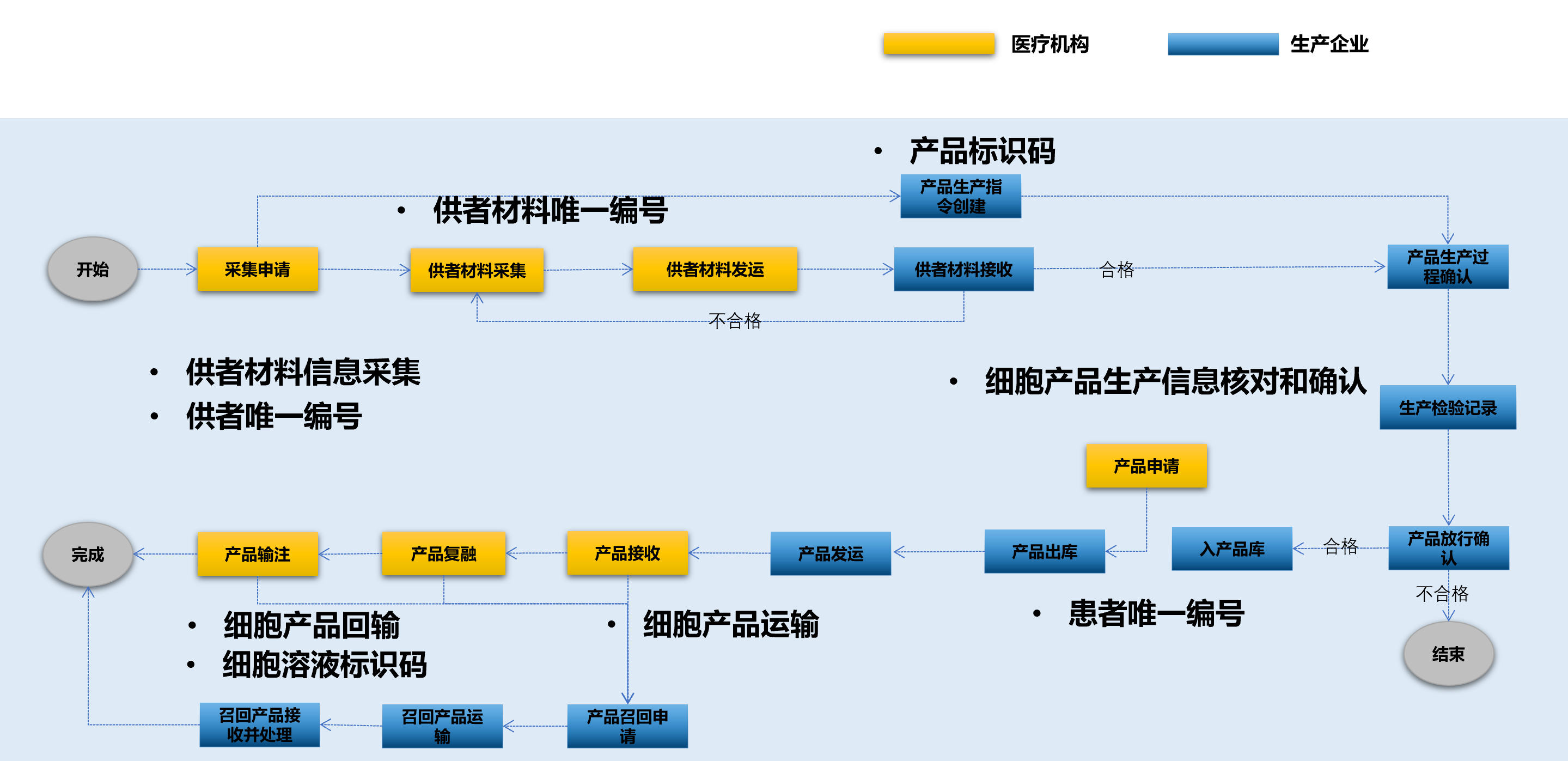
2. 供者材料采集与运输:详细规定了从供者材料采集申请到运输全过程的管理要求,确保供者材料的可追溯性。
3. 产品生产:涵盖了从供者材料接收到产品放行的全过程,实现生产环节的全程可控。
4. 产品存储、申请与运输:规定了产品入库、出库、运输计划等环节的管理要求,保证产品流转过程的可追踪。
5. 产品使用:包括产品接收、复融和输注等环节,确保产品使用过程的安全性和可追溯性。
6. 产品召回:规定了产品召回的全流程管理,提高了不良事件的应对能力。
7. 产品信息追溯:支持通过多种标识码查询产品全生命周期信息,实现了全方位的追溯能力。
《细胞治疗产品追溯管理信息系统基本功能规范》标准的发布对细胞治疗产品追溯具有重要意义:
1. 实现全程可追溯:通过统一的信息系统、用于标识供者材料和产品的唯一性的编号,实现从供者材料采集到产品使用的全过程追溯,实现产品从供者到患者或从患者到供者的双向追溯。
2. 实现数据防混淆:在从供者材料采集到产品使用的全过程中,确保可识别供者且具有唯一性的编号不会发生标识错误或遗漏,确保供者材料或细胞产品与患者之间的匹配性。
3. 提高数据安全性:通过严格的身份认证、权限管理和审计追踪,保障了系统和数据的安全性,同时也保护了供者和患者的隐私。
4. 规范行业标准:为细胞治疗产品追溯管理信息系统的开发和应用提供了统一的标准,有利于行业的规范化发展。
5. 落实法规要求:该标准源于《细胞治疗产品生产质量管理指南(试行)》,将法规要求具体化、操作化,便于企业和医疗机构执行。
6. 提升应急能力:通过完善的召回机制,提高了对不良事件的快速响应能力,最大限度地保障患者安全。
《细胞治疗产品追溯管理信息系统基本功能规范》标准的发布,是我国细胞治疗领域质量管理体系建设的重要一步。这一标准为产品追溯系统提供了具体的技术参考,有助于企业更好地落实相关法规要求。它不仅为行业提供了可操作的参考,也为提升细胞治疗产品全生命周期的可追溯性创造了条件。我们期待看到,随着这一标准的逐步实施,细胞治疗产品质量管理和患者安全保障方面取得新的进展。