乳腺癌概况
据国家癌症中心预估:2022年我国乳腺癌发病人数接近43万,居恶性肿瘤第5位;死亡人数接近26万,排名第7位;而病死率在女性患者中均高居第1位,成为威胁女性生命健康的头号杀手[1]。值得关注的是,2017年我国乳腺癌发病人数较1990年增加了2.63倍,有效的预防筛查与诊断治疗刻不容缓[2]。
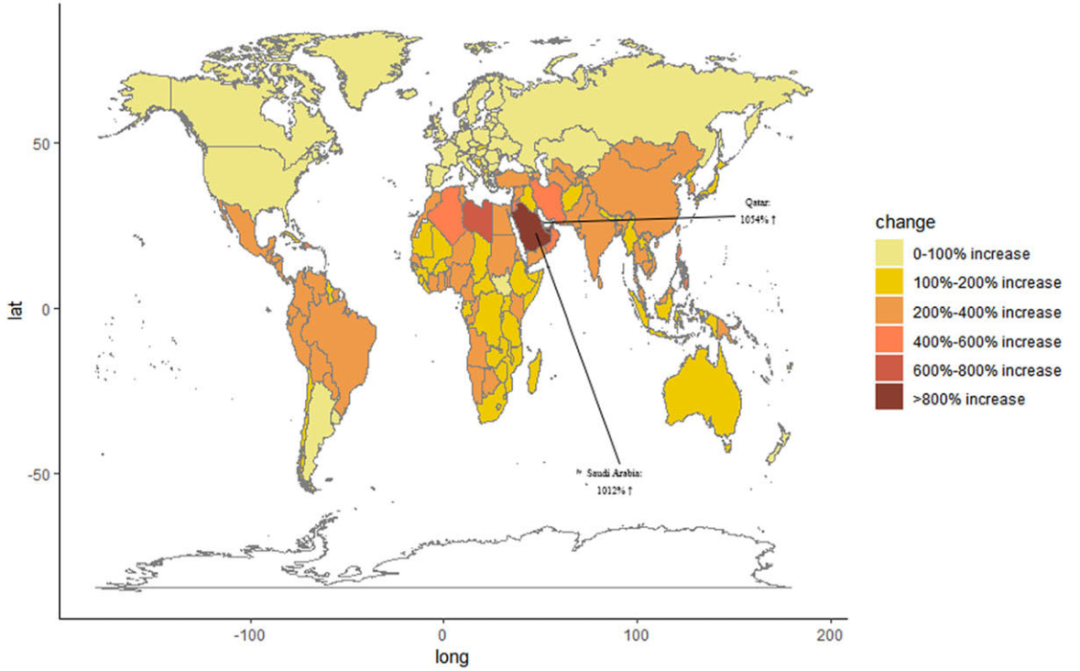
图1. 1990年至2017年乳腺癌相对发病率变化[2]
我国晚期(IV期)的乳腺癌患者虽然仅占4.7%,但早期患者在接受规范治疗后却有约40%的比例最终进展为晚期,而晚期患者的5年生存率仅21%,这部分患者的生存面临严峻挑战[3]。
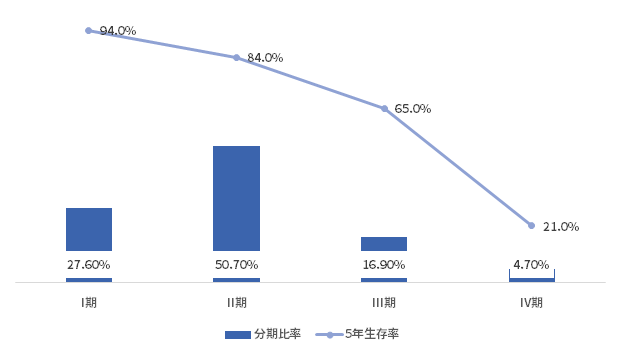
图2. 不同分期的生存率[3]
乳腺癌有三种常见的分子亚型:激素受体阳性(HR+)、HER2阳性(HER2+)和三阴性乳腺癌,其中绝大部分为HR+型乳腺癌。乳腺癌可以进一步细分为五种分子亚型(如图3),其中LuminaA型预后最好,HER2+型次之,三阴性乳腺癌的预后最差[4]。
另外,乳腺癌的不同亚型之间,呈现出了特异的分子特征:如Luminal A型以ESR1、GATA3、FOXA1异常居多;Luminal B型的PIK3CA突变率高达40%;HER2+型显然有较高的HER2扩增比例;三阴型的TP53、BRCA突变较为常见,而且PD-L1也有一定的表达概率[5]。针对各亚型的分子特征,出现了多种个体化诊疗方案。
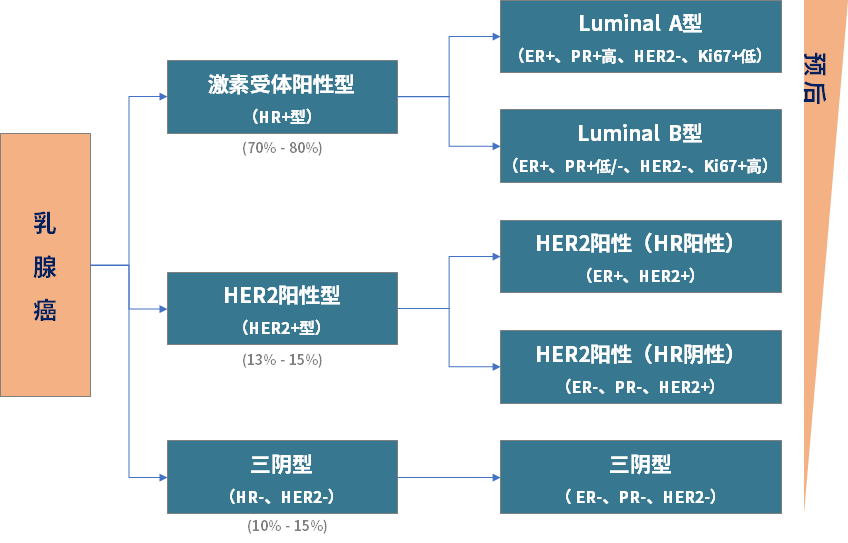
图3. 乳腺癌分型及预后[4]
乳腺癌诊疗路径
CSCO指南对于乳腺癌的三个主要亚型均匹配了个性化诊疗方案(如图4),但目前也面临一些困境。比如HR+型乳腺癌晚期推荐PIK3CA的检测,但目前该靶点药物Alpelisib并未在国内上市;HER2+型乳腺癌患者有多种HER2抗体药物选择,但该亚型靶标单一(仅HER2);而目前三阴型乳腺癌的治疗方案较为丰富,有PARP抑制剂(需要检测BRCA1/2、HRR基因、HRDscore)以及免疫检查点抑制剂(需要检测PD-L1表达或者TMB),这为占比~15%的且预后最差的三阴乳腺癌患者的预后改善提供了强有力的弹药。
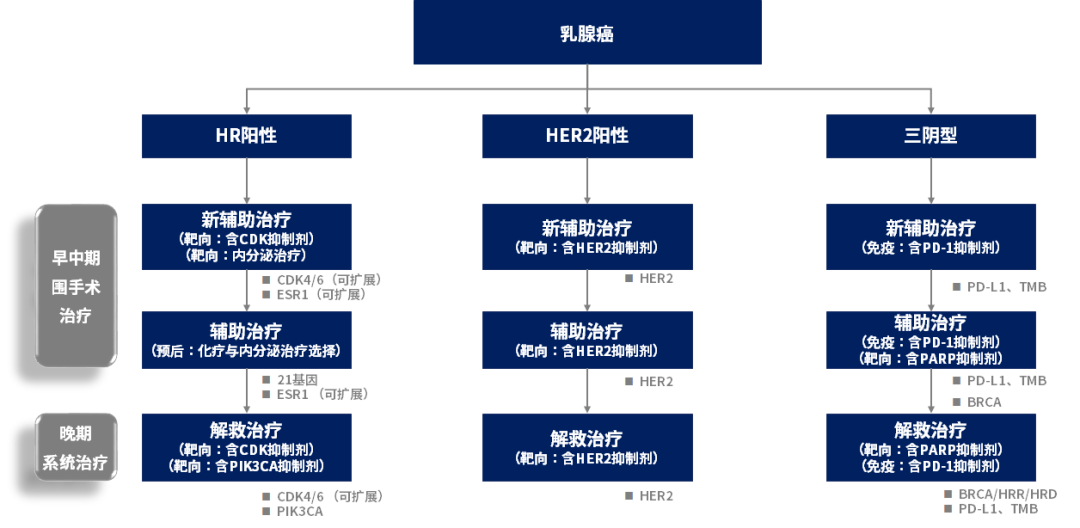
图4. 乳腺癌诊疗路径[4]
三阴性乳腺癌的抗PD-(L)1治疗
参考2022年CSCO乳腺癌临床诊疗指南,仅帕博利珠单抗联合方案可以用于新辅助、辅助及晚期一线治疗,其他的PD-(L)1药物的使用建议入组临床试验。然而最早在三阴乳腺癌中获批(FDA)的免疫方案为阿替利珠单抗联合白蛋白紫杉醇,只是至今未在国内(NMPA)批准[6]。
另外需要强调的是,CSCO指南要求晚期三阴乳腺癌一线免疫方案需要明确PD-L1的状态,即PD-L1阳性患者方可接受帕博利珠单抗治疗。

图5. 三阴性乳腺癌抗PD-(L)1治疗方案[4] [6]
三阴性乳腺癌中PD-L1检测的价值
前文提到,CSCO乳腺癌临床诊疗指南要求晚期一线免疫治疗方案需要明确PD-L1的状态。这是基于KEYNOTE-355的一项随机、双盲III期临床试验,研究目的是通过帕博利珠单抗(K药)+化疗方案和安慰剂+化疗方案的比较,评估帕博利珠单抗联合化疗用于三阴性乳腺癌患者的效果。其中,K药+化疗组的中位无进展生存期(mPFS)均优于安慰剂+化疗组,且随着PD-L1表达(Combined Positive Score, CPS)的提升而延长:当不做PD-L1筛选时的mPFS为7.5个月(图6, C),当PD-L1阳性(CPS≥1)时的mPFS为7.6个月(图6, B),当PD-L1阳性(CPS≥10)时的mPFS为9.7个月(图6, A),并以CPS≥10作为最终阈值[7]。
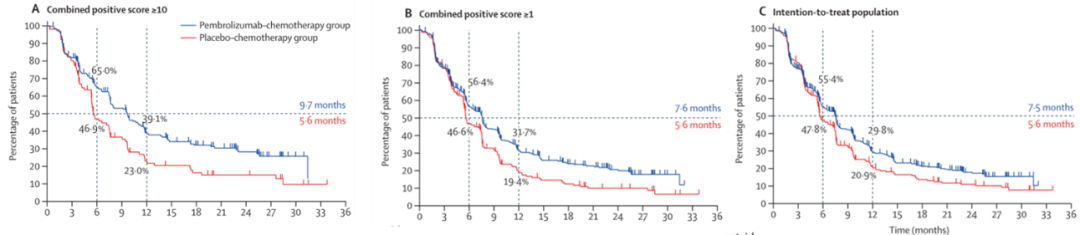
图6. K药+化疗组 vs 安慰剂+化疗组的生存比较[7]
迈杰医学PD-L1抗体试剂
迈杰医学是一家拥有多组学、多平台的综合型创新企业,致力于解决创新药物的研发痛点及患者的用药痛点,助力精准医疗。业务覆盖药企服务、伴随诊断试剂开发和肿瘤用药指导检测服务,国内外合作客户已将近300家。迈杰医学拥有独立的病理中心,可提供一站式病理学解决方案,包括:全套的Leica组织样本制备系统,Ventana、Leica、Dako等全自动免疫组化仪,3D HISTECH Pannoramic MIDI数字化病理扫描仪及91360远程病理系统,具备从样本制备到H&E,IHC、FISH、RNAscope及多重免疫组化(mIHC)等全套组织病理和分子病理检测能力,并有专业的病理医生提供相应的阅片或远程病理阅片服务,目前已完成50+靶点的方法学建立,30+靶点的方法学验证。迈杰医学的PD-L1抗体试剂(产品名:迈普康),是一款经免疫组织化学方法用于免疫检查点抑制剂伴随诊断标志物PD-L1蛋白表达检测的试剂盒,预期通过检测非小细胞肺癌患者FFPE样本的PD-L1表达情况,可辅助用于指导纳武利尤单抗等免疫检查点抑制剂使用。

图7. 迈普康产品特点
参考文献
[1]Chin Med J (Engl). 2022 Feb 9;135(5):584-590.
[2] J Hematol Oncol. 2019 Dec 21;12(1):140.
[3] Lancet Public Health. 2021 Dec;6(12):e877-e887.
[4] CSCO乳腺癌临床诊疗指南,2022.
[5] Nat Rev Dis Primers. 2019 Sep 23;5(1):66.
[6] https://www.fda.gov/drugs/resources-information-approved-drugs/oncology-cancer-hematologic-malignancies-approval-notifications
[7] 2020 Dec 5;396(10265):1817-1828.